
EMSA探針設計
經典EMSA是使用放射性同位素(一般為P32)標記探針。由于P32的短壽命與放射性,用P32標記探針只能經實驗者全手工用末端轉移酶或激酶進行標記。 如果順利,2天左右能獲得探針,但10多天后又要重新進行標記。市場上的EMSA探針末端標記產品適合于同位素標記,對非放射性標記沒有什么用。
現在已很少有人用P32標記探針做EMSA了。非放射性EMSA探針常采用生物素,熒光或地高辛(DIG)。非放射性分子標記EMSA探針的最大好處是可以 在核酸合成過程中進行標記,具有高效,省時,費用低的優點。
一、非放射性探針制作需掌握下面幾點:
(1)文獻查找與分析:1)如果利用實驗者自測的基因序列做EMSA,需要對其進行分析尋找TF結合序列,并與文獻進行比對。2)在文獻中可以查
到大多數TF的結合序列,但最好進行交叉驗證以防出錯。
3)需要注意文獻發表的探針序列可能并不適合做非放射性EMSA(見下面解釋)。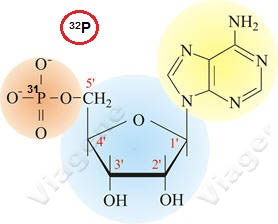
(2)探針設計:須注意
1)防止探針封閉成環,2)防止錯位配對,3)排除目標序列以外結合位點的,4)防止產生空間位阻,5)適當考慮AT/GC比例,6)一般EMSA探針只有幾十堿基對。探針太長會產生過多結合位點導致結果分析困難,還會產生超級螺旋結構而掩蓋結合部位。
(3)核酸合成:1)合成量不能太少,量太少不準確,易產生多余的單鏈。2)需要HPLC純化。3)如果是RNA探針,要防止降解。
(4)生物素或熒光標記:1)建議采用Biotin或紅外熒光標記,盡量不要采用DIG標記。2)標記只能在探針末端。3)為提高靈敏度,探針兩端都須有標記。
(5)質譜分析:用質譜對探針進行純度與分子量分析,以防出錯。
(6)雙鏈制作:對配對的單鏈需進行仔細計算,確保互補鏈為等當量反應。探針中的多余單鏈所引起高背景,使非特異帶增加,致結果分析困難。
(7)比活性測定:新制作的探針需要稀釋后才能直接用于EMSA。稀釋度是通過將新探針做不同稀釋度后與已知量探針進行比活性測定來確定的。
(8)制作應用液:按比活性確定稀釋倍數,用TE稀釋制作探針應用液,-20保存。
二、探針空間位阻問題:
在32P標記的探針中,磷酸基團是DNA本身的結構。用放射性P32代替P31的最大的好處是探針標記只增加了1個電子(圖1),對探針的化學結構與結合能力的影響可忽略不計,EMSA結果最恒定。
我們比較放射性與非放射性EMSA時發現一些轉錄因子用P32探針能夠出結果,但改用非放射性探針后就不能出結果。
一些轉錄因子用放射性探針與非放射探針的EMSA結果不一致。我們的進一步分析顯示探針用非放射性分子標記導致結果不一致的主要原因。對核酸探針而言,
非放射性標記物都屬于外加分子(圖2為生物素標記物,圖3為熒光分子標記物)。為提高靈敏度,常常在探針兩端都進行標記。標記后的分子都會使原來的探針增加至少1000-2000道爾頓。如果采用文獻報道的長度為20-22堿基(6-7千道爾頓)的EMSA探針,
標記物占探針分子的比例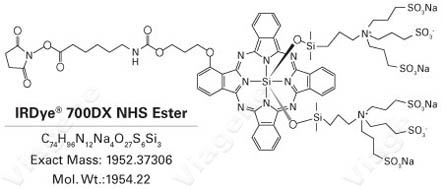 很高。另一方面,用生物素標記的探針在與TF結合后還需要有足夠空間與Avidin-HRP(分子量~100K)結合。此外,外加的標記物還可能影響到探針的電荷狀態,形成聚合物,出現沉淀。
很高。另一方面,用生物素標記的探針在與TF結合后還需要有足夠空間與Avidin-HRP(分子量~100K)結合。此外,外加的標記物還可能影響到探針的電荷狀態,形成聚合物,出現沉淀。
由于我們的產品開發是從放射性EMSA過度到非放射性EMSA的,我們有條件將非放射性探針進行各種比較,并找出可能解決方案并進行驗證。我們發現一些探針需改變長度,一些需變更結合,一些需加入非離子去污劑才能獲得滿意結果。一些客戶做不出理想EMSA,探針問題可能是其中一個重要原因。

 客服一號
客服一號
